7-6 电镀原理及应用

电镀是在含有待镀金属离子的水溶液中电解电镀产品作为阴极(-极)和待镀金属作为阳极(+极)的过程。主要用于增加装饰性、耐腐蚀、耐磨等目的,如镀金(Au)、镀锌(Zn)、镀铬(Cr)、镀镍(Ni)等。
如图1所示,电镀的原理是在阴极发生还原反应,金属析出并作为镀膜生长。即,电解液中的金属离子[Mn + ]接受电子[ne-],作为金属[M]在表面析出。阳极发生氧化反应,阳极的金属溶解在镀液中,补充镀液中的金属离子。这样,当被镀金属作为阳极时,阳极溶解在电解液中,故称为可溶性电极。另一方面,也使用不溶于镀液的阳极(不溶性电极)。
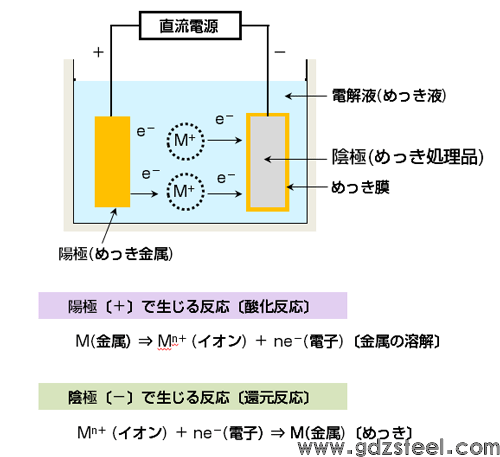
图1 电镀原理
电解液可以镀上含有金属离子的金属盐溶液,但添加剂在获得有光泽和致密的薄膜方面起着重要作用。例如,为了使镀膜有光泽,需要使用光亮剂,添加表面活性剂以抑制凹坑的产生。
如图2所示,电镀工序按照前处理工序、主处理工序、后处理工序的顺序进行,但为了保证足够的附着力,前处理工序尤为重要。在预处理过程中,根据被加工产品的加工历史和材料选择更佳方法。例如,酸洗对于那些有氧化皮的人来说是必不可少的。作为清洗工序,进行溶剂清洗、碱清洗、电解清洗等,在电镀前进行酸浸(表面活化)。活化后以镀锌为主要处理工艺的电镀工艺,但大部分镀镍和镀铬在进行主要处理工艺之前都用铜代替(罢工镀)。
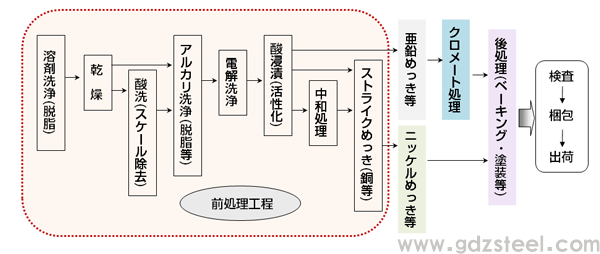
图 2 电镀工艺示例
表 1 显示了机械零件常用的 Zn、Ni 和 Cr 电镀的电镀液(电解液)。镀锌是为了防止钢材生锈和腐蚀,由于价格便宜,所以用于螺栓等许多机械部件。镀液使用含有氢氧化钠的碱性青色镀液、含有氯化钾或氯化铵的酸性镀液等。由于锌镀层本身的耐腐蚀性较差,镀后通常进行铬酸盐处理。铬酸盐处理提供防腐和装饰效果,如光泽、淡黄色、黄色和绿色。
表1 电镀的主要电镀液
| 镀膜 | 浴池名称 | 主成分 | |
|---|---|---|---|
| 锌 (Zn) | 碱性浴 | 青色浴 | 氰化锌 [Zn (CN) 2 ]、氰化钠 [NaCN]、氢氧化钠 [NaOH] |
| 银手浴 | 氧化锌 [ZnO]、氢氧化钠 [NaOH] | ||
| 氯化物浴 | 氯化钾浴 | 氯化锌 [ZnCl 2 ]、氯化钾 [KCl]、硼酸 [H 3 BO 3 ] | |
| 氯化铵浴 | 氯化锌 [ZnCl 2 ]、氯化铵 [NH4Cl]、硼酸 [H 3 BO 3 ] | ||
| 镍 (Ni) | 笏浴 | 硫酸镍 [NiSO 4 ]、氯化镍 [NiCl 2 ]、硼酸 [H 3 BO 3 ] | |
| 氨基磺酸浴 | 氨基磺酸镍 [Ni (SO 3 ) 2 · H 2 O]、氯化镍 [NiCl 2 ]、硼酸 [H 3 BO 3 ] | ||
| 铬 (Cr) | 萨金特浴 | 铬酸酐 [CrO 3 ]、硫酸 [H 2 SO 4] | |
| 氟化物浴 | 铬酸酐[CrO 3 ]、硫酸[H 2 SO 4 ]、氟硅酸钠[Na 2 SiF 6 ] | ||
镀镍具有高硬度和优异的光泽和耐腐蚀性,因此被用于许多领域。此外,如图3所示,为了提高耐腐蚀性和附着力,通常在基材上镀铜。作为镀液,使用硫酸镍或氨基磺酸镍作为主要成分。

图 3 镀镍 (Ni) 产品的横截面示例
此外,在铝及其合金镀镍时,铝的表面被稳定的氧化物覆盖,因此除非去除氧化物,否则无法实现具有优异附着力的镀层。因此,如图3的镀膜截面所示,在这种情况下,使用通过锌酸盐处理的Zn置换镀。在该Zn置换镀之后,进行Cu镀等,在更终工序中进行作为主要工序的Ni镀。
镀铬包括膜厚0.5μm以下的装饰性镀铬和膜厚2~100μm的工业镀铬。特别是工业镀铬的硬度为800~1000HV,因此常被用作汽车零件、模具、机床轴等的硬镀铬。但是,虽然镀硬铬具有优异的耐磨性和抗脱模性,但在400℃以上硬度急剧下降,因此不能在使用过程中温度升高的地方使用。
由于镀铬薄膜的残余应力为拉应力,残余应力随着薄膜厚度的增加而增加,从而在薄膜和薄膜表面产生裂纹。这对于工业镀铬薄膜来说是不可避免的,因为它是薄膜的一种自我防御措施,试图缓解残余应力。例如,图 4 显示了工业镀铬膜表面的裂纹状态及其横截面结构。这些裂纹的存在不利于耐腐蚀性,但由于具有润滑剂保持作用,所以在润滑环境中使用时非常有效。

图 4 工业铬 (Cr) 镀膜中存在的裂纹
原文链接:优钢网 » 7-6 电镀原理及应用




发表评论